 順天堂大学大学院 医学研究科 代謝内分泌内科学の遅野井雄介助教、三田智也准教授、綿田裕孝教授らの研究グループはこのほど、血管障害にオートファジー(タンパク分解機構の一つ)が重要な役割を果たしていることを発見した。
順天堂大学大学院 医学研究科 代謝内分泌内科学の遅野井雄介助教、三田智也准教授、綿田裕孝教授らの研究グループはこのほど、血管障害にオートファジー(タンパク分解機構の一つ)が重要な役割を果たしていることを発見した。
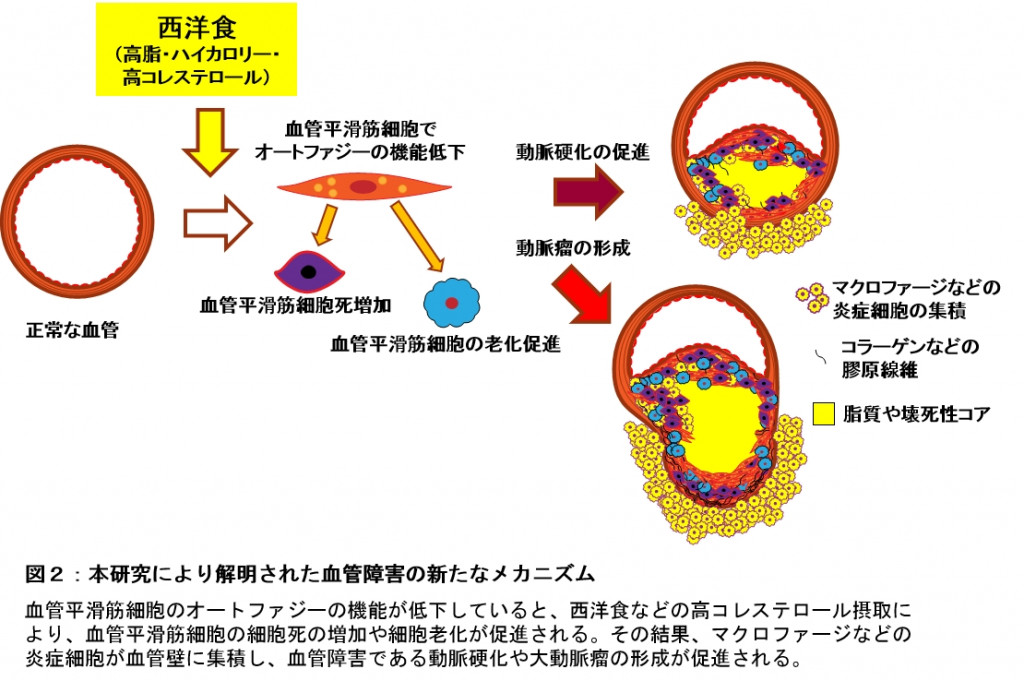
オートファジー不全モデルマウスの解析により、血管平滑筋細胞のオートファジーの機能低下が細胞死や細胞老化を引き起こし、西洋食の摂取による動脈硬化の進展と大動脈瘤の形成を促進することがわかった。これらの結果は、血管平滑筋細胞のオートファジー機能の亢進が血管障害の予防治療の新たな標的となる可能性を示唆しているという。
研究グループは、まず、オートファジーに必須な遺伝子の一つであるatg7を平滑筋細胞で欠損させた平滑筋細胞特異的オートファジー不全マウス(Atg7欠損マウス)を作製。次に、動脈硬化症のモデルマウスとして知られているApoE欠損マウスを掛け合わせることで血管平滑筋細胞特異的オートファジー不全モデルマウス・ApoE欠損マウス(KOマウス)を作製した。
このマウスに西洋食(14週間、1.25%コレステロール)を摂取させると、KOマウスの死亡率が著明に増加した。死亡例の中には、胸部大動脈瘤が破裂していたことが死因と考えられるマウスもいた。KOマウスの大動脈を観察すると、腹部大動脈周囲には慢性炎症が生じており、動脈硬化巣が増加していた。この動脈硬化巣では、壊死性コアの拡大や薄い線維性被膜の形成など不安定プラークの特徴を示す所見が認められた。
興味深いことに、KOマウスの病理像はヒトの動脈硬化巣と極めて類似していた。また、動脈硬化巣では細胞死(アポトーシス)が増加しており、動脈硬化巣の拡大やプラークの不安定化に関与していると考えられた。
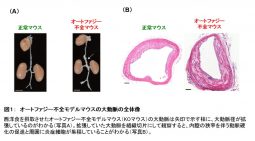 一方で、血管壁では細胞死に伴う中膜平滑筋細胞数の減少、中膜弾性線維の破壊や動脈瘤様に拡張している部位など血管壁の脆弱性に関連する所見が確認された。さらに詳細な検討から、血管平滑筋細胞のオートファジー機能が低下すると細胞死が増加することや、p53経路(細胞周期に関わる)が活性化され、細胞老化が促進されることがわかった。
一方で、血管壁では細胞死に伴う中膜平滑筋細胞数の減少、中膜弾性線維の破壊や動脈瘤様に拡張している部位など血管壁の脆弱性に関連する所見が確認された。さらに詳細な検討から、血管平滑筋細胞のオートファジー機能が低下すると細胞死が増加することや、p53経路(細胞周期に関わる)が活性化され、細胞老化が促進されることがわかった。
これに続いて、炎症性マクロファージが血管壁に集積し、血管壁構造の破壊を引き起こしていることが判明した。
以上の結果から、血管平滑筋細胞におけるオートファジー機能不全は、細胞死や細胞老化を介して、血管障害である動脈硬化の進展や大動脈瘤の形成を促進することがわかったとしている。